Para os menos atentos as cores dos LEDs são obtidas da mesma forma que nas lâmpadas comuns: a luz é branca e basta colocar um plástico da cor desejada para se ter luz vermelha, verde, amarelo, ou qualquer outra. Na verdade, o LED não é uma lâmpada incandescente mas sim um semicondutor e a cor da sua luz é determinada por um processo muito mais complexo que explicamos neste artigo. Entender como a produção de luz ocorre num simples LED pode ser muito importante para que os leitores entendam mais sobre a física dos semicondutores e que rege o funcionamento de uma grande quantidade de dispositivos que vão desde os simples diodos até os lasers.
A luz nada mais é do que radiação eletromagnética, ou seja, é formada por ondas cujas frequências se diferenciam dos sinais comuns de rádio, TV, radar e outros que estamos acostumados a usar em eletrônica, apenas pela sua frequência. Na figura 1 temos a colocação da faixa visível, ou seja, das frequências que nossos olhos podem ver, no espectro eletromagnético.
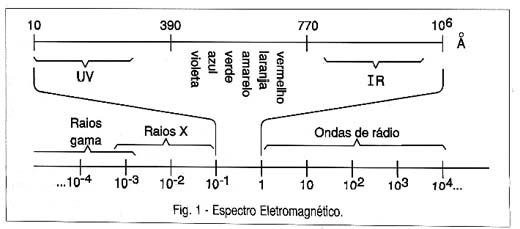
Conforme o leitor pode perceber, nesta faixa, os diversos comprimentos de onda ou frequências determinam também o tipo de sensação que nosso olho vai ter em relação à cor da luz.
Assim, as frequências mais baixas e portanto os comprimentos de onda maiores correspondem à luz vermelha e laranja, enquanto que os comprimentos de onda menores e frequências mais altas correspondem a radiação azul e violeta.
A maneira mais simples de se obter luz e portanto a emissão de radiação eletromagnética é pelo aquecimento. Aquecendo um corpo, seus átomos vibram em todas as frequências possíveis emitindo luz de todas as cores que se misturam. O sol opera desta forma e uma lâmpada comum de filamento também.
No sol a elevada temperatura agita os átomos das substâncias que o formam de tal maneira que eles passam a emitir radiação o mesmo ocorrendo com o filamento de uma lâmpada incandescente quando percorrido por uma corrente elétrica, conforme mostra a figura 2.
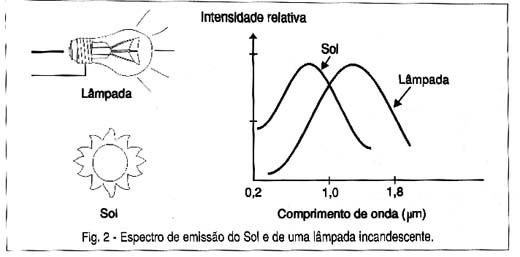
A emissão de radiação destes corpos é feita desordenadamente. Isso significa que, cada átomo ao ser agitado, emite uma pequena porção de radiação num comprimento de onda ou frequência diferente.
É interessante observar que a energia emitida nestas condições também tem uma quantidade mínima, como o átomo que é a porção mínima de matéria. Isso significa que os átomos excitados sempre emitem essas porções mínima, que são denominadas "quantum" de energia. O plural de "quantum", que é uma palavra latina, é "quanta" e a teoria que explica como elas se comportam é a teoria quântica.
Assim, quando os átomos são agitados pelo calor, cada qual emite um "quantum" de energia de frequência diferente. O resultado disso é que não temos um único tipo de radiação, mas sim uma mistura que cobre todo o espectro visível e mesmo parte do que não podemos ver como das radiações infravermelhas e ultravioleta, conforme mostra a figura 3.
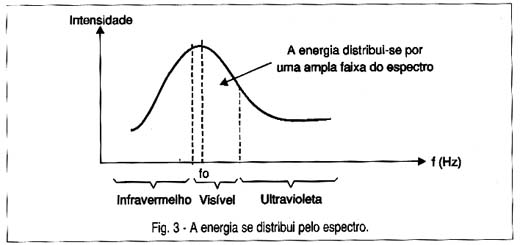
Se a distribuição da energia emitida, ou seja, a quantidade de quanta for mais ou menos uniforme no setor do espectro que podemos ver, a mistura nos dará a sensação de uma luz branca.
Ora, a distribuição dessa energia emitida varia conforme a temperatura do corpo. Um corpo mais quente tende a emitir mais partículas de frequências mais elevadas. Por este motivo, um corpo muito quente brilha com luz azulada. Já um corpo mais frio, por exemplo, um ferro em brasa, brilha com luz avermelhada, conforme mostra a figura 4.
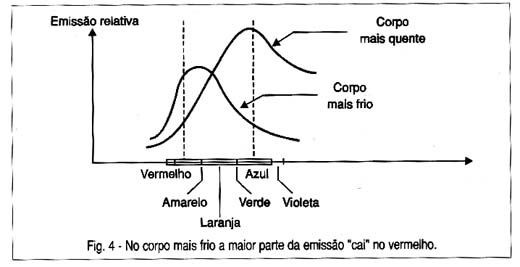
Um físico chamado Boltzman estabeleceu numa fórmula a distribuição da emissão dessa radiação em função da temperatura para um corpo negro.
O interessante de uma emissão de luz branca, ou que contenha todos os comprimentos de onda como a do sol é que ela nos permite ver as cores da natureza.
Assim, o que ocorre é que se iluminarmos um objeto e ele refletir apenas a luz azul, absorvendo as demais, ele vai nos parecer azul, conforme mostra a figura 5.
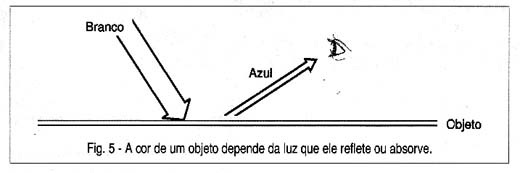
Os objetos que vemos na natureza quando iluminados pela luz do sol ou de uma lâmpada comum aparecem nas cores que tem porque refletem as frequências que determinam essas cores.
Se iluminarmos um objeto verde com uma fonte de luz que emita radiação apenas correspondente à luz vermelha, o objeto vai nos parecer completamente negro.
Veja então que podemos falar em dois tipos de emissões de luz:
A das fontes como o Sol e uma lâmpada comum que na realidade possuem todas as frequências possíveis e que portanto cobrem uma faixa larga do espectro e de fontes que podem emitir luz de uma única frequência.
Em eletrônica podemos associar estas fontes de uma única frequência a um transmissor bem sintonizado enquanto que a de luz que cobre o espectro todo seria um emissor de ruído.
Dizemos que as fontes de luz que emitem radiação de uma única frequência ou cor são monocromáticas. Os LEDs são fontes monocromáticas porque produzem sua luz por um processo diferente do que vimos para o Sol e para uma lâmpada comum. Analisemos como os LEDs funcionam:
NÍVEIS DE ENERGIA E LUZ MONOCROMÁTICA
Qualquer material, inclusive os semicondutores, quando são aquecidos emitem luz pela agitação de seus átomos.
Entretanto, certos materiais podem emitir luz sem serem aquecidos, ou seja, podem emitir luz mesmo que frios, por um processo denominado luminescência.
A luminescência de certos materiais é conhecida desde 1889 mas somente há pouco tempo tem sido mais usada na eletrônica na criação de diversos dispositivos.
Um tipo de luminescência é a que ocorre quando um feixe de elétrons bate contra uma camada de fósforo na tela de um televisor. A luminescência é explicada da seguinte forma:
Os elétrons que giram em torno de um átomo o fazem em órbitas bem estabelecidas que fixam níveis de energia, conforme mostra a figura 6.
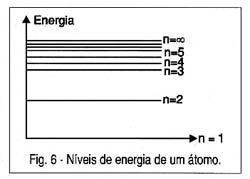
Um átomo pode absorver por um breve instante energia e quando isso ocorre um elétron "salta" de sua órbita passando para outra de maior nível energético. Em outras palavras, a energia fica armazenada potencialmente na posição do elétron em sua órbita.
Quando o elétron, uma fração de segundo depois de absorver a energia, volta para sua órbita normal, a energia absorvida é devolvida, conforme mostra a figura 7.
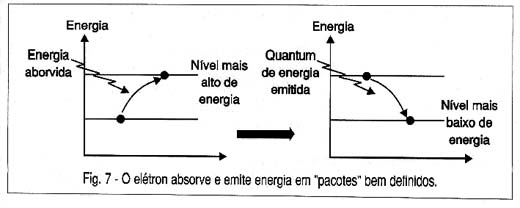
A energia devolvida é um quantum de radiação eletromagnética cuja frequência vai depender do "salto" do elétron, ou seja, da energia que ele tem para devolver.
Os níveis de energia que um elétron pode assumir num átomo dependem da natureza deste átomo, ou seja, do material que ele representa. Assim, para cada tipo de átomo os elétrons só podem dar saltos definidos, o que significa que eles só podem devolver a energia na forma de radiação eletromagnética de frequência muito bem definida.
Se a faixa de energia que o elétron devolver estiver entre 3800 e 7500 Angstrons, a energia se manifesta na forma de luz visível e o material em que isso ocorre passa a emitir luz.
Existem diversas formas de se excitar um material para que ele absorva e depois emita a energia na forma de radiação eletromagnética.
A circulação de uma corrente no sentido direto por uma junção semicondutora, por exemplo, um diodo comum, conforme mostra a figura 8, é uma delas.
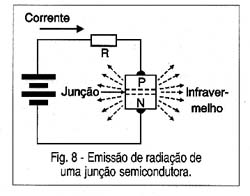
No entanto, num diodo comum, a energia emitida está concentrada na faixa do infravermelho (que não podemos ver) e sua intensidade é muito pequena.
Esta radiação tem sua frequência justamente determinada pela natureza do material semicondutor usado nos diodos que é o silício.
Para se obter radiação em frequências mais altas que a do infravermelho pode-se empregar outros materiais semicondutores que tenham níveis de energia diferentes e até mesmo mudar estes níveis pela adição de impurezas.
Assim, como o Arseneto de Gálio semicondutor (GaAs) conseguimos um rendimento maior no processo, mas ainda na faixa do infravermelho.
Agregando fósforo ou índio ao arseneto de gálio podemos obter frequências maiores e o semicondutor já passa a emitir luz na faixa do vermelho, amarelo, laranja, verde, azul e chegar até o violeta e ultravioleta, conforme mostra o gráfico da figura 9.
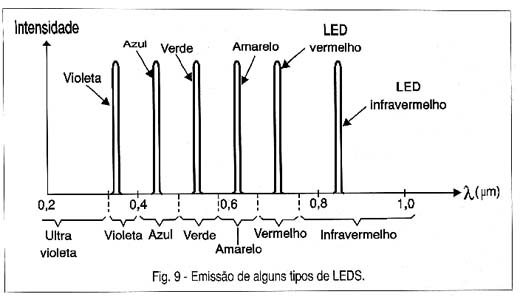
Veja por este gráfico que as curvas de emissão dos dispositivos obtidos desta forma que são os LEDs (Light-Emitting Diodes ou Diodos Emissores de Luz) são bastante estreitas o que significa que eles são fontes de luz monocromáticas.
Para obter frequências mais elevadas que a da luz verde, uma nova substância tem sido usada. Trata-se do Carbeto de Silício (SiC) que tem propriedades luminescentes conhecidas desde o início do século.
No entanto, a obtenção de cristais semicondutores puros desta substância foi uma dificuldade superada somente há pouco tempo.
O Carbeto de Silício na forma de semicondutor pode, ao ser excitado eletricamente, emitir luz não só na faixa de frequências correspondente ao azul como chegar até mesmo ao violeta.
Desta forma, com esta nova substância podem ser fabricados LEDs azuis e violetas que já estão no mercado. Outra substância que também apresenta a emissão de luz na faixa do violeta é o Nitreto de Silício (SiN) que também já é usado na fabricação de LEDs.
Na figura 10 temos a estrutura de um LED deste tipo, em que se observa a existência de três tipos de materiais.
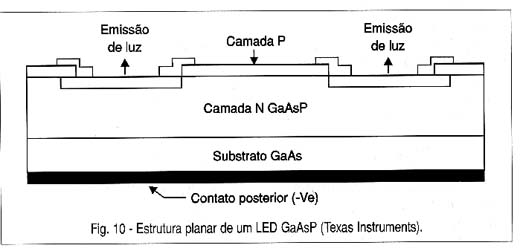
Juntamente com a junção pn epitaxial temos um substrato de SiC que é excitado na condução e que provoca a emissão da luz.
Na figura 11 temos a curva de emissão de um LED azul observando-se que ela é bem mais larga que a dos LEDs comuns de Arseneto de Gálio, dadas as próprias características do material semicondutor.
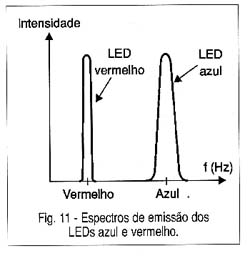
Os LEDs azuis e violetas possuem uma curva característica semelhante a de qualquer diodo e LED comum, apenas com o "joelho", ou seja, o ponto de início da condução numa tensão um pouco mais alta: 2,5 V.
Esta curva característica é mostrada na figura 12, e ela nos mostra que o uso de um LED deste tipo em nada difere dos LEDs comuns, sendo necessária a colocação de um resistor limitador de corrente em série.
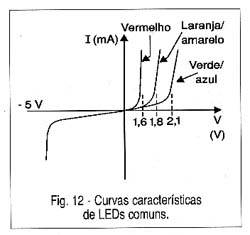
LASERS SEMICONDUTORES
O que diferencia um Laser de um LED é que no LASER a luz emitida é concentrada e coerente, devido ao próprio processo de produção no material semicondutor.
Num LED a luz é produzida por uma excitação descontrolada dos átomos que, ao receber e devolver a energia emitem luz a qualquer instante e em qualquer direção.
Num LASER os átomos recebem a excitação de tal forma que haja um fenômeno denominado "inversão de população", ou seja, que em determinado instante tenhamos mais átomos excitados do que sem excitação.
Assim, quando um átomo devolve sua energia forma de um quanta de luz, este quanta serve para excitar outros átomos energizados, forçando-os a devolver sua energia numa espécie de reação em cadeia, mostrada na figura 13.
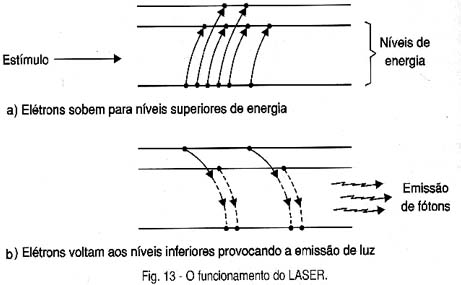
O resultado é que a devolução da energia absorvida se faz de forma excitada e coordenada o que resulta na emissão de luz concentrada e coerente.
Um espelhamento no material semicondutor permite que esta devolução seja mais controlada e a emissão ocorra na forma de feixe numa direção única.
Mas, da mesma forma que nos LEDs a frequência e portanto a cor da luz emitida depende da natureza do material e hoje já estão disponíveis LASERs semicondutores de diversos comprimentos de onda.