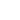Os primeiros LEDs emitiam apenas radiação infravermelha. Não havia tecnologia para se obter a emissão de luz em frequências mais elevadas, o que exigia maior energia. Somente com o tempo os LEDs foram sendo aperfeiçoados chegando a faixa do ultravioleta. Hoje são comuns e encontram uma infinidade de aplicações práticas. Veja como isso funciona.
No nosso artigo “A cordos LEDs” (veja o link) mostramos como os LEDs produzem luz. Vimos que a luz dos LEDs é obtida pela mudança dos níveis de energia dos elétrons num átomo.
Um átomo pode absorver por um breve instante energia e quando isso ocorre um elétron "salta" de sua órbita passando para outra de maior nível energético. Em outras palavras, a energia fica armazenada potencialmente na posição do elétron em sua órbita.
Quando o elétron, uma fração de segundo depois de absorver a energia, volta para sua órbita normal, a energia absorvida é devolvida, conforme mostra a figura 1.
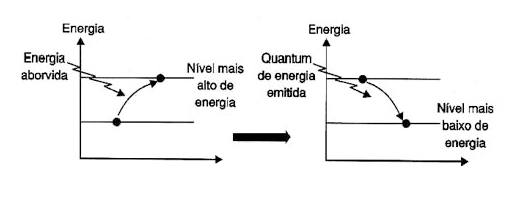
A energia devolvida é um quantum de radiação eletromagnética cuja frequência vai depender do "salto" do elétron, ou seja, da energia que ele tem para devolver.
Os níveis de energia que um elétron pode assumir num átomo dependem da natureza deste átomo, ou seja, do material que ele representa. Assim, para cada tipo de átomo os elétrons só podem dar saltos definidos, o que significa que eles só podem devolver a energia na forma de radiação eletromagnética de frequência muito bem definida.
Se a faixa de energia que o elétron devolver estiver entre 3800 e 7500 Angstrons, a energia se manifesta na forma de luz visível e o material em que isso ocorre passa a emitir luz.
Existem diversas formas de se excitar um material para que ele absorva e depois emita a energia na forma de radiação eletromagnética.
A circulação de uma corrente no sentido direto por uma junção semicondutora, por exemplo, um diodo comum, conforme mostra a figura 2, é uma delas.
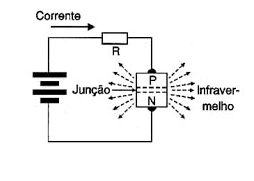
No entanto, num diodo comum, a energia emitida está concentrada na faixa do infravermelho (que não podemos ver) e sua intensidade é muito pequena.
Esta radiação tem sua frequência justamente determinada pela natureza do material semicondutor usado nos diodos que é o silício.
Para se obter radiação em frequências mais altas que a do infravermelho pode-se empregar outros materiais semicondutores que tenham níveis de energia diferentes e até mesmo mudar estes níveis pela adição de impurezas.
Assim, como o Arseneto de Gálio semicondutor (GaAs) conseguimos um rendimento maior no processo, mas ainda na faixa do infravermelho.
Agregando fósforo ou índio ao arseneto de gálio podemos obter frequências maiores e o semicondutor já passa a emitir luz na faixa do vermelho, amarelo, laranja, verde, azul e chegar até o violeta e ultravioleta, conforme mostra o gráfico da figura 3.
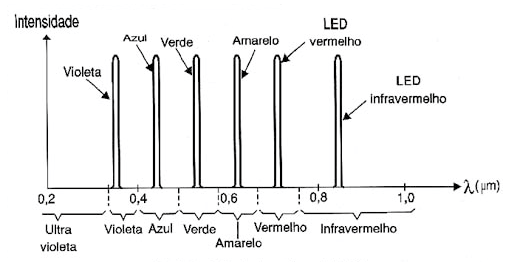
Veja por este gráfico que as curvas de emissão dos dispositivos obtidos desta forma que são os LEDs (Light-Emitting Diodes ou Diodos Emissores de Luz) são bastante estreitas o que significa que eles são fontes de luz monocromáticas.
LEDs ultravioletas
Para obter frequências mais elevadas que a da luz verde, uma nova substância tem sido usada. Trata-se do Carbeto de Silício (SiC) que tem propriedades luminescentes conhecidas desde o início do século. No entanto, a obtenção de cristais semicondutores puros desta substância foi uma dificuldade superada somente há pouco tempo.
O Carbeto de Silício na forma de semicondutor pode, ao ser excitado eletricamente, emitir luz não só na faixa de frequências correspondente ao azul como chegar até mesmo ao violeta.
Desta forma, com esta nova substância podem ser fabricados LEDs azuis e violetas que já estão no mercado. Outra substância que também apresenta a emissão de luz na faixa do violeta é o Nitreto de Silício (SiN) que também já é usado na fabricação de LEDs.
Na figura 4 temos a estrutura de um LED deste tipo, em que se observa a existência de três tipos de materiais.
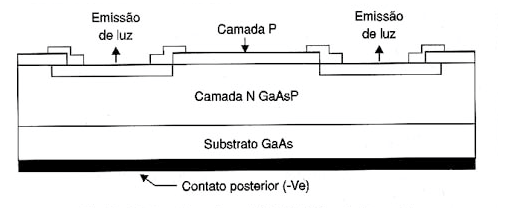
Juntamente com a junção pn epitaxial temos um substrato de SiC que é excitado na condução e que provoca a emissão da luz.
Na figura 5 temos a curva de emissão de um LED azul observando-se que ela é bem mais larga que a dos LEDs comuns de Arseneto de Gálio, dadas as próprias características do material semicondutor.
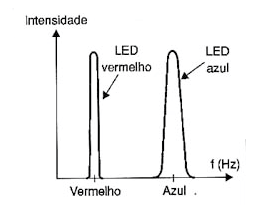
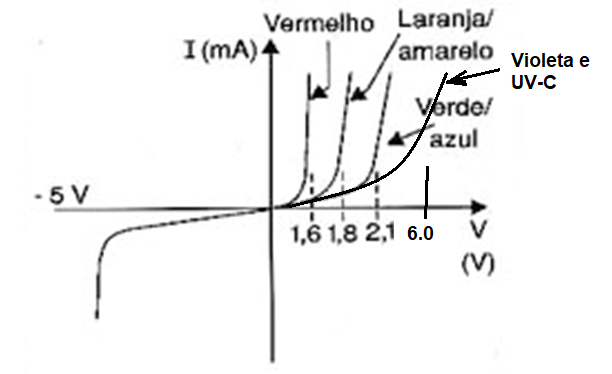
Os LEDs possuem uma curva característica semelhante a de qualquer diodo e LED comum, apenas com o "joelho", ou seja, o ponto de início da condução numa tensão um pouco mais alta: de 2,5 V chegando aos 6 V para os UVC.
Esta curva característica é mostrada na figura 6, e ela nos mostra que o uso de um LED deste tipo em nada difere dos LEDs comuns, sendo necessária a colocação de um resistor limitador de corrente em série.
Usos
A radiação ultravioleta, por ter mais energia, pode manifestar efeitos sobre seres vivos de uma forma mais intensa, por exemplo, com efeitos bactericidas.
Assim, os LEDs ultravioletas encontram uma ampla gama de aplicações em biologia. Podemos citar o tratamento da água, como agente biológico de desinfecão e na química na curagem de polímeros.
Para cada aplicação existem comprimentos de onda apropriados havendo, portanto, uma divisão das faixas de frequência do ultravioleta em A, B e C com aplicações específicas e LEDs para cada caso.
Normalmente, nos tipos dos LEDs é especificada a faixa como LED-A, LED-B ou LED-C, (figura 7)
As aplicações das diversas faixas são:
Classificações de espectros UV, seu uso e benefícios:
• UV-C (200-280 nm): Quase completamente absorvido pela atmosfera da Terra, UV-C é comumente usado por seus efeitos germicidas
• UV-B (280-320 nm): Aproximadamente 95% de UV-B é absorvido pelo
atmosfera da Terra e é frequentemente conhecido por sua associação com
aumento do risco de câncer de pele, no entanto, também demonstrou ter
efeitos antimicrobianos, incluindo lidar com infecções agrícolas e pragas,
como oídio ou ácaros; bem como acionar a planta
respostas que aumentam os flavonóides e canabinóides
• UV-A (320-400 nm): Frequentemente chamada de “luz negra”, a luz UV-A tem o comprimento de onda mais longo no espectro UV e é considerado o menos
prejudicial; é mais conhecido por aplicações em cura UV, detecção de falsificação forense, mas também tem aplicações para a agricultura devido à sua capacidade de desencadear as respostas desejadas da planta.
Link: https://www.newtoncbraga.com.br/index.php/como-funciona/1000-a-cor-dos-leds-art142
https://compoundsemiconductor.net/article/112266/The_Evolution_Of_The_Deep-UV_LED/feature