O aprendizado das ciências naturais pode ser melhorado com a visualização de fenômenos através de experiências. É claro que a maioria das escolas não possui recursos para a realização de experiências até relativamente simples, em vista do custo do equipamento, mas existem soluções alternativas econômicas que merecem análise. Mostraremos algumas.
Este artigo é destinado aos professores de ciências, física e química do nível médio que desejam ter um rendimento muito maior em suas aulas, com a realização de experiências interessantes, que possam ilustrar os fenômenos estudados.
Os equipamentos próprios para a realização de muitos experimentos são caríssimos e inexistem na maioria das escolas, mas descrevemos uma alternativa de baixo custo para a realização de experiências no campo da físico-química e eletroquímica.
Além de muito simples de montar, os efeitos Obtidos são bastante atraentes, despertando inclusive o interesse dos alunos por esta área do conhecimento.
Futuros cientistas são gerados a partir de experiências muito simples de iniciação e nosso país precisa disso!
Utilizando apenas uma lâmpada comum e um diodo (que pode até ser aproveitado de velhos aparelhos), descrevemos uma fonte experimental para experiências de físico-química e algumas das interessantes demonstrações que professores (e alunos) podem realizar.
A montagem também é válida como sugestão de excelente trabalho para feiras de ciências.
O equipamento
O equipamento consiste simplesmente em duas peças ligadas, de modo a formar uma fonte de corrente contínua.
De fato, na tomada de energia temos corrente alternada e sem limitação alguma de intensidade, o que além de inconveniente para as experiências é até perigoso.
O que fazemos então é usar uma lâmpada comum de 25 watts a 60 watts para limitar a corrente e um diodo semicondutor para retificar.
Na figura 1 temos o diagrama completo do nosso "equipamento".
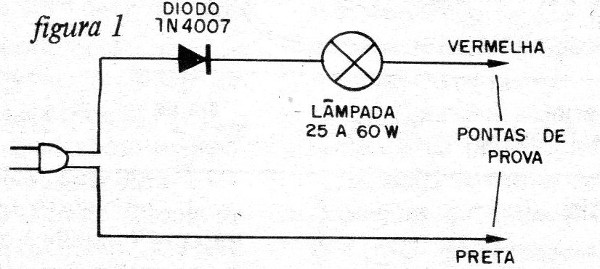
Sua montagem pode ser feita numa base de madeira, conforme mostra a figura 2.
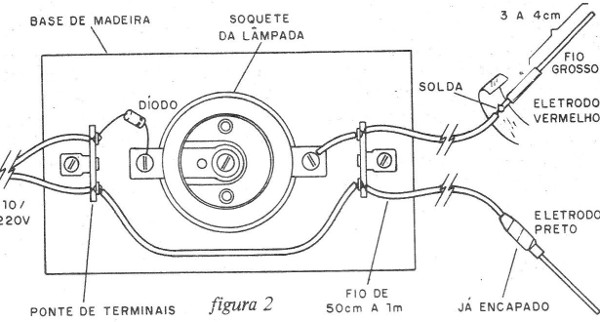
As pontas de prova nada mais são do que dois pedaços de fios grossos, em que desencapamos aproximadamente 3 ou 4 cm de um dos extremos.
No outro extremo de cada ponta, soldamos o fio de ligação e isolamos o lugar com fita isolante, para maior segurança.
É muito importante que as partes metálicas do aparelho não fiquem expostas, pois um contacto acidental pode provocar choque ou curto-circuito.
Prova inicial
Tendo montado seu aparelho, para provar basta ligar o cabo de alimentação na tomada de força.
Coloque a lâmpada no suporte e encoste uma ponta de prova na outra. A lâmpada deve acender. (figura 3)
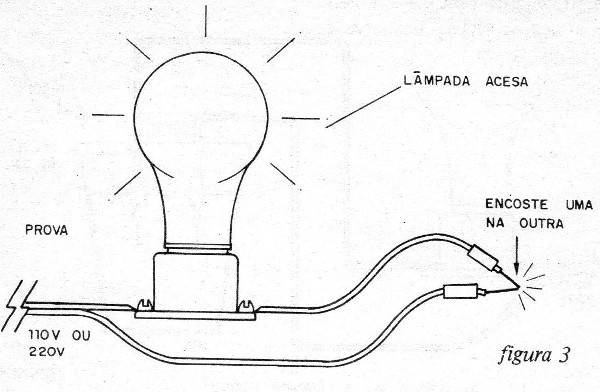
O que ocorre neste caso é que há continuidade no circuito que se fecha, e uma corrente contínua passa a alimentar a lâmpada.
Observe que a lâmpada acende com aproximadamente metade de seu brilho total. Isso ocorre porque o diodo só deixa passar, metade dos semiciclos da alimentação.
Experiência 1 – Condutividade de soluções
Com esta experiência o professor pode demonstrar que a água pura é um bom isolante e que a água com sais, ácidos ou bases dissolvidos, torna-se condutora de eletricidade.
Num copo com água comum (ou água destilada), colocamos os eletrodos do nosso equipamento conforme mostra a figura 4.
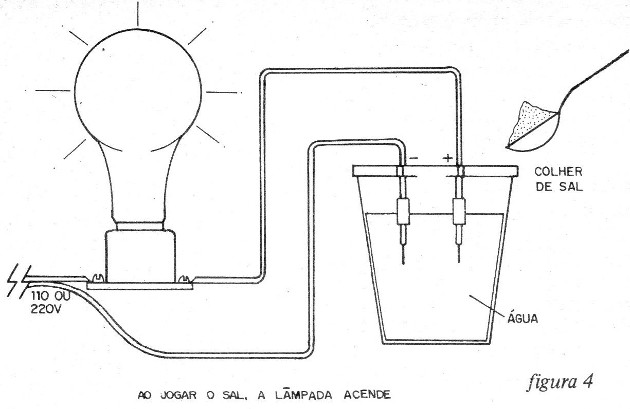
A água da torneira ou de fontes não é quimicamente pura, nem mesmo a água da chuva que contém muitas impurezas, de modo que ambas não são isolante perfeito.
A lâmpada pode mostrar sinais de aquecimento do seu filamento que chega a "avermelhar" em alguns casos. O ideal é usar água destilada, mas a água comum também proporciona resultados satisfatórios, pois sua concentração de impurezas é pequena.
A lâmpada na configuração inicial, estará completamente apagada, mas no momento em que jogarmos uma colher de sal ou outras substâncias na água, haverá a imediata transformação de suas propriedades e ela se tornará condutora, fazendo a lâmpada acender.
Explique aos alunos que o acendimento da lâmpada se deve ao fato da água se tornar condutora nas condições indicadas e não ao fato dela estar gerando qualquer forma de energia.
Experiência 2 - Eletrólise
Deixando os eletrodos na solução (água e sal) a corrente que vai circular provoca reações químicas interessantes. Estas reações que ocorrem com a ajuda de correntes elétricas são denominadas “eletrólise".
Depois de alguns minutos ligado, o aparelho vai tornar a água turva com coloração azulada, além da formação de saís no fundo do copo.
Estes sais são devidos à decomposição do cobre que se combina com o cloro (do sal), resultando em sais como o cloreto de cobre e outros que os professores de química podem melhor explicar escrevendo as reações envolvidas.
Experiência 3 - Formação de hidrogênio
A eletrólise da água pode ser feita se em lugar de dissolvermos sal no copo com este líquido, utilizarmos uma pequena quantidade de ácido sulfúrico (que pode ser conseguido em farmácias ou no laboratório da escola).
Cuidado ao trabalhar com o ácido! Pingue somente algumas dezenas de gotas com cuidado no copo! Neste caso, as borbulhas que saem do polo negativo (ponta preta), serão de hidrogênio e as que saem do polo positivo, serão de oxigênio. (figura 5)
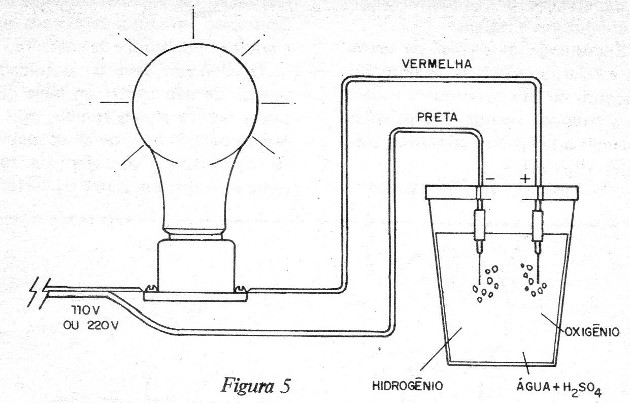
A turvação da solução se deve à reações que ocorrem com o cobre dos eletrodos (na verdade o seu desgaste exige que periodicamente eles sejam trocados).
A reação de formação dos gases a partir da água é:
2H2O ? 2H2 + O2
Um aperfeiçoamento para esta experiência consiste em se utilizar como eletrodos, carvões retirados de pilhas gastas com cuidado e devidamente limpos.
Neste caso, não ocorre a reação que corrói o eletrodo.
Experiência 4 - Ignição elétrica
Esfregue os eletrodos num pedaço de Bombril e veja o resultado!
A queima instantânea deste material pelo efeito da corrente. (figura 6)
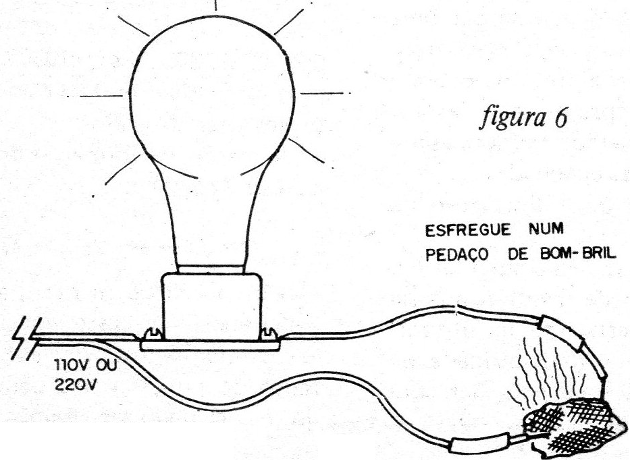
O que ocorre é que a corrente que circula pelos finos filamentos da esponja de aço, provoca seu aquecimento (efeito térmico da corrente) e consequente inflamação.
Soprando o material durante a experiência, gera-se combustão completa da esponja de aço.
Experiência 5 – Identificação de condutores e isolante
Encostando as pontas de prova em diferentes materiais poderemos descobrir se são condutores (quando a lâmpada acende) ou isolantes (quando a lâmpada permanece apagada). (figura7)
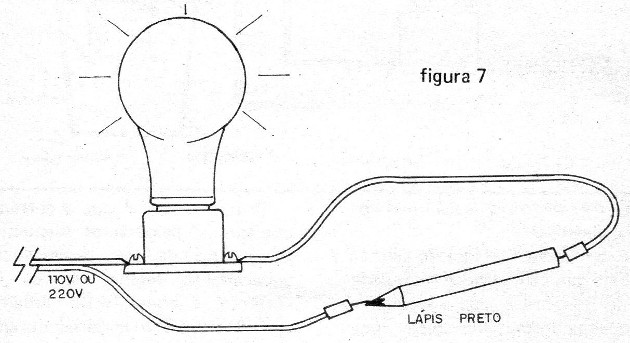
Em especial, recomendamos a realização da experiência com um lápis, caso em que se comprova que a grafite é condutora de corrente.
O professor deve ter o cuidado apenas de não pegar um lápis que tenha levado algum tombo, pois a grafite partida no interior da madeira interrompe a passagem da corrente e a experiência não dá certo.
Publicado Originalmente em 1990