Este artigo de 2009 descreve uma tecnologia então criada pela Philips para diagnóstico por imagem. O artigo foi publicado na época com base em documentação fornecida pela própria Philips.
Uma nova tecnologia de tomografia permite obter imagens tridimensionais do interior do corpo humano. O método criado pela Philips é denominado MPI ou Magnetic Particle Imaging conseguindo obter imagens muito melhores do que as imagens 2D até então obtidas com a tecnologia anterior. O método in vivo foi apresentado revelando imagens incomparáveis em tempo real do fluxo sangüíneo e dos movimentos cardíacos, o que pode aprimorar o diagnóstico por imagem e o planejamento do tratamento;
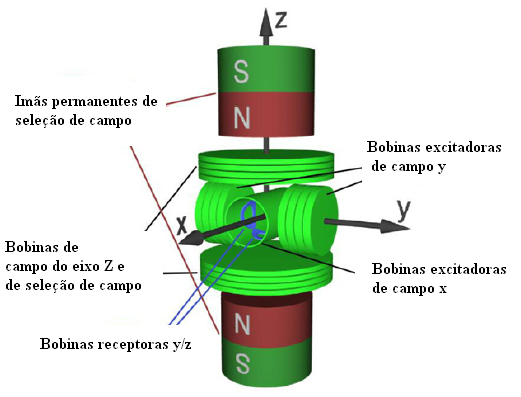
Os primeiros resultados práticos desta nova tecnologia foram apresentados em São Paulo no final de fevereiro Em um estudo pré-clínico da tecnologia, usando as propriedades magnéticas de nanopartículas de óxido de ferro injetadas na corrente sanguínea, ela gerou imagens em tempo real do fluxo arterial e dos movimentos cardíacos volumétricos. Isso representa um grande passo adiante na transformação dessa tecnologia de um conceito teórico em uma ferramenta de diagnóstico por imagem do corpo inteiro para ajudar a melhorar o diagnóstico e o planejamento da terapia das principais doenças do mundo, como ataque cardíaco, AVC e câncer. Os resultados dos estudos pré-clínicos foram publicados na edição 54 da revista Physics in Medicine and Biology (2009). Na figura 1 temos uma visão simplificada do scanner utilizado nesta nova tecnologia.
O MPI da Philips usa as propriedades magnéticas de nanopartículas de óxido de ferro injetadas para medir sua concentração no sangue. Como o corpo humano não contém nenhum material magnético produzido naturalmente, não há outro sinal magnético que interfere no MPI. Após a injeção, as nanopartículas logo aparecem como sinais claros nas imagens, a partir das quais suas concentrações podem ser calculadas. Integrando alta resolução espacial a tempos de aquisição de imagem menores (normalmente na casa de 1/50 de segundo), o MPI pode capturar variações de concentração dinâmicas à medida que as nanopartículas passam pela corrente sangüínea. Isso pode permitir aos equipamentos de MPI realizar várias avaliações cardiovasculares funcionais de uma só vez. Entre essas avaliações podem estar o fluxo de sangue coronário, a perfusão miocárdica e o volume de ejeção cardíaca, além do movimento das paredes cardíacas e da velocidade do fluxo.
Como funciona
O scanner mostrado na figura 1 tem uma dimensão de orifício de 32 mm. Um par de imas permanentes e um par de bobinas produzem a seleção de gradientes de campo. Os gradientes são respectivamente de 3 e 2,5 Tum-1.Este gradiente ocorre no eixo vertical . Três conjuntos de bobinas permitem a obtenção de imagens 3D. As bobinas de seleção de campo verticais produzem um campo de 18mTuo. Os dois campos excitadores em direções ortogonais são produzidos por bobinas de seleção de campo dedicadas. As frequências dos campos são escolhidas de modo a mover o FFP numa trajetória Lissajous 3D. As frequências para as três orientações são de 2,5 MHz/99 = 22,25 kHz, 2,5 MHz/96 = 26,04 kHz e 2,5 MHz/102 = 24,51 kHz. A trajetória de Lissajous tem um tempo de repetição de 21 ms o que corresponde a codificação de 42 volumes por segundo cobrindo um volume de 20,4 x12 x 16,8 mm3. O tamanho das aberturas do padrão de Lissajous foi escolhido de modo a se obter uma resolução de 1 mm. O receptor é formado por duas bobinas que são alinhadas de um modo aproximadamente perpendicular uma em relação a outra e ao orifício Na direção axial o solenóide que produz o campo também é utilizado na recepção.
Um novo conceito de receptor foi implementado para reduzir o ruído por um fator dependente da frequência entre 5 e 100. Num scanner ideal, o ruído na cadeia receptora é gerado pelas flutuações de corrente no paciente, enquanto na realidade, os ruídos nas bobinas e no circuito receptor também contribuem para o nível de ruído. O MRI aceita o ruído do paciente, porque a faixa estreita do sinal permite a migração do ruído do amplificador por casamento ressonante
No MRI para se obter a redução do ruído , foi projetado um amplificador refrigerado a líquido com JFETs com uma entrada de tensão de apenas 80 pV Hz-1/2 e uma capacitância de entrada de 1 nF em toda a faixa relevante de frequência de 50 kHz a 1 MHz. Além disso as tensões de ruído das bobinas receptoras sozinhas são de 50 pV/Hz -1/2 o que resulta num ruído total de 100 pV/Hz -1/2. Os valores de sinal extremamente baixos exigem realmente circuitos com características especiais.
Os leitores que dominam o inglês podem encontrar no artigo científico "Three dimensional real time in vivo magnetic particle imaging" publicado na edição 54 da revista Physics in Medicine and Biology (2009), o qual pode ser baixado em http://stacks.iop.org/0031-9155/54/L1 (*), as informações completa sobre o assunto.