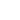O silício é o elemento número 14 da tabela de classificação periódica, tendo peso atômico 28 e consistindo num metalóide tetravalente (4 elétrons na última camada da valência). O silício se enquadra no grupo dos materiais semicondutores sendo a base de toda a eletrônica moderna. Dopado com impurezas ele se torna um semicondutor do tipo P ou N, e suas junções resultam em comportamento elétricos que são a base dos componentes modernos. Assim, com ele são fabricados componentes como diodos, transistores, circuitos integrados e muitos outros. Na figura 1 temos a estrutura de um átomo de silício. Observe que existem 14 prótons e 14 nêutrons no núcleo, o qual é circundado por 14 elétrons sendo 4 na camada de valência.
O silício é encontrado em abundância na crosta terrestre na forma de dióxidos (sílica ou silicatos), consistindo no segundo elemento mais abundante do planeta. Esses compostos de silício são usados na fabricação de vidros, cimentos e cerâmicas, também sendo constituindo dos produtos conhecidos como silicones. Os silicones são substâncias plásticas formados por silício, oxigênio, carbono e hidrogênio.
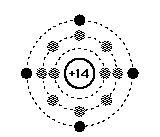
Na forma pura, o silício forma uma estrutura metálica de cor cinza e brilho metálico. Essa estrutura é formada por cristais. Na figura 2 temos a estrutura de um cristal de silício.
O silício foi descoberto por Lavoisier em 1787 e seu nome vem do latim significando “rocha dura”. Na indústria automotiva existem muitos compostos importantes do silício que são usados nos mais diversos produtos tais como:
Dióxido de Silício (SiO2)
Silicatos
Carboneto de silício (SiC)
Nitreto de silício (Si3N4)
Tetracloreto de silício (SiCl4)
Silicones
Os silicones, em especial são usados na fabricação de graxas resistentes a alta temperatura, selantes, vedação, abrasivos, vidros, etc. Além disso, são usados em explosivos e em pirotecnia além de implantes.