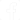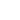Uma das experiências mais interessantes apresentadas em trabalhos escolares, e que também serve para ilustrar a ação da eletricidade nas reações químicas, é a eletrólise. Nas versões tradicionais são usadas pilhas como fontes de energia, porém estas apresentam o terrível defeito de se esgotarem rapidamente, e no preço que estão... Para eliminar este problema e fazer uma eletrólise numa versão mais moderna, apresentamos uma fonte de baixa tensão com limitação de corrente.
Obs. Este artigo originalmente foi publicado no livro Experiências e Brincadeiras com Eletrônica Jr. Vol 2 de 1985, mas sendo o tema atual foi revisado para ser novamente levado aos leitores.
A eletrólise nada mais é do que a decomposição da água em seus elementos formadores, ou seja, o hidrogênio e o oxigênio.
Conforme sabemos da química, a fórmula H2O indica que a água é formada por duas partes de hidrogênio e uma parte de oxigênio, ou seja, estes gases entram na proporção de 2 para 1.
Para “extrair" o oxigênio e o hidrogênio da água existe um método que faz uso da corrente elétrica e é denominado ”eletrólise".
Na eletrólise da água ocorre uma reação de decomposição que pode ser escrita como:
2H2O => 2H2 + O2
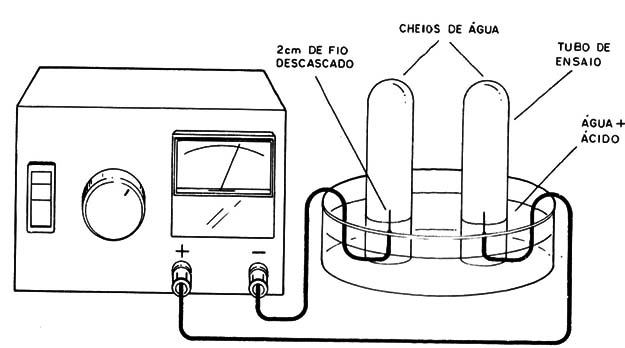
Na prática, é muito simples fazer a eletrólise da água, conforme mostra a figura 1.
Numa cuba de vidro (qualquer recipiente serve) colocamos água, de preferência pura, isto é, destilada, já que a água de torneira ou de poço contém muitos sais minerais dissolvidos que prejudicariam a experiência.
Como a água pura é isolante da eletricidade, temos de dissolver algo que a torne condutora, mas que não entre na reação, atrapalhando-a.
Este algo é o ácido sulfúrico (H2SO4) que pode perfeitamente ser usado na proporção de 1:20, ou seja, uma parte de ácido para cada 20 de água que for empregada.
Depois, nesta cuba são colocados dois fios elétricos desencapados com suas pontas voltadas para cima, nas quais prendemos dois tubos de ensaio (tubos de laboratório, que podem ser adquiridos em farmácias) invertidos e cheios de água inicialmente.
Ligamos nos fios uma fonte de energia elétrica contínua qualquer como, por exemplo, algumas pilhas. A corrente começará a circular pelos fios e pela solução (água + ácido) tendo então início a reação.
O leitor verá então que das pontas dos fios se desprendem minúsculas bolhas de gás que sobem e ficam retidas dentro dos tubos, conforme mostra a figura 2.
O hidrogênio tem uma "tendência" positiva, enquanto o oxigênio tem uma "tendência" negativa, o que quer dizer que enquanto o primeiro é atraído para o polo negativo o outro é atraído para o polo positivo. No fio negativo as bolhas são de hidrogênio e no fio positivo as bolhas são de oxigênio.
A quantidade de gás que se desprende é função da intensidade da corrente e pode perfeitamente ser prevista através de fórmulas.
Assim, pelas leis de Faraday, temos que uma carga elétrica de 96 500 Coulombs libera um equivalente químico de determinada substância, onde este equivalente químico é definido como peso atônico de um elemento dividido por sua valência.
Para o caso do hidrogênio, pode- mos raciocinar do seguinte modo:
Um Coulomb representa a carga transportada por uma corrente de 1 ampère em cada segundo. Como a massa atômica deste elemento é 1 e sua valência também, temos que, em cada segundo, a corrente de 1 ampère liberará uma massa de:
m = 1/96 500
m = 1,036x 10-5 g
Ou, se quisermos saber, por hora, basta multiplicar por 3 600:
m = 0,037 g
UMA FONTE PARA ELETRÓLISES
Conforme o leitor deve ter percebido, o importante numa eletrólise é a intensidade da corrente.
Sendo assim, a tensão atua apenas como um meio de forçar esta corrente, em função das dimensões dos eletrodos usados, trabalhando-se em geral com tensões baixas.
No nosso caso, a tensão poderá ser variada entre 0 e 12 V, aproximadamente, e em condições normais a corrente chegará até 1A, o que é bem mais do que o obtido de pilhas comuns.
Na figura 3 temos a estrutura de nossa fonte.
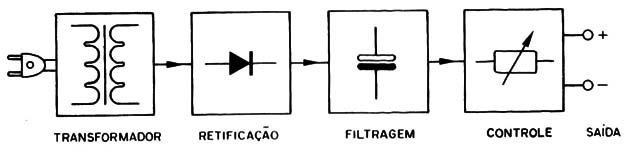
Começamos pelo transformador que abaixa a tensão da rede para os 12 V sob correntes de até 1A, isolando também a cuba onde é realizada a experiência, com muito mais segurança para o experimentador.
Como a eletrólise deve ser frita com corrente contínua, devemos retificá-la, o que é conseguido com a ajuda de dois diodos.
Após o diodo temos, em primeiro lugar, uma pequena filtragem, feita por um capacitor eletrolítico, e depois uma etapa de controle que utiliza um transistor de potência e um potenciômetro comum. É neste potenciômetro que ajustaremos a corrente para cada experiência.
O transistor funciona como uma espécie de torneira, deixando passar apenas a corrente que é ajustada pelo potenciômetro. Em vista desta ação, este componente tende a se aquecer, devendo por isso ser montado num radiador de metal.
Na saída temos um limitador de corrente que consiste num resistor e também um instrumento que permite avaliar com boa precisão qual é a corrente que está passando pela cuba.
O instrumento é do tipo de bobina móvel usado em aparelhos de som como VU-meter, sendo por isso de baixo custo e fácil obtenção.
Os leitores que não sejam propriamente ligados à eletrônica e os menos experientes não terão dificuldades em montar esta fonte de eletrólise, pois daremos todas as explicações pormenorizadamente.
A MONTAGEM
Uma caixa, conforme mostra a figura 4, pode ser usada para alojar todos os componentes.
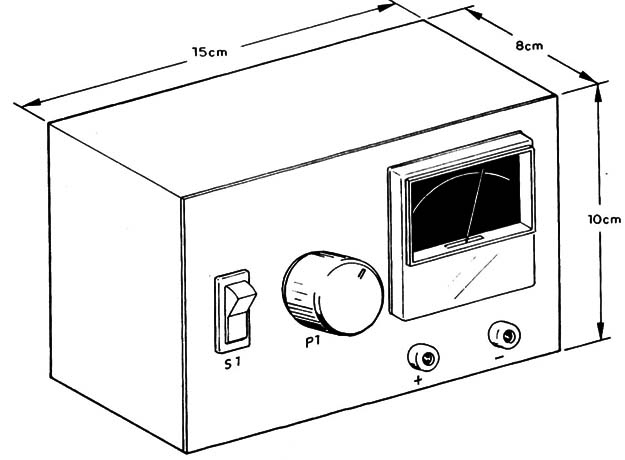
Esta caixa poderá ser de metal, plástico ou mesmo de madeira.
O circuito completo da fonte para eletrólise e mostrado na figura 5.
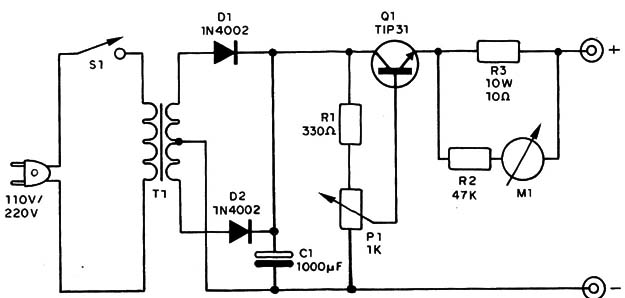
Usaremos como chassi, para soldar os componentes menores, uma ponte de terminais que será fixada na própria caixa (se não for de metal) ou numa base de madeira, tudo conforme mostra a figura 6.
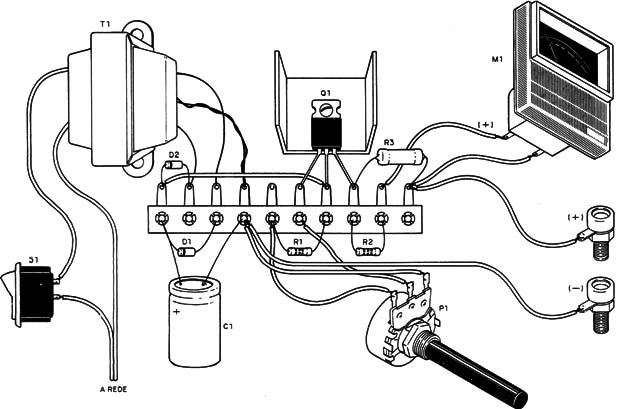
Nesta figura temos então a maneira exata como devem ser soldados todos os componentes. Sugerimos que os leitores sigam a sequência abaixo para não cometerem nenhum erro.
a) Solde em primeiro lugar o transistor na ponte de terminais, tendo o cuidado de fixar antes o seu radiador de calor que consiste numa chapinha de metal dobrada. Se puder, ajude a fixação do transistor com a colocação adicional de um parafuso no dissipador de calor que o prenda à base.
b) Os próximos componentes a serem soldados são os diodos, D1 e D2. Devemos observar bem sua posição, seguindo a posição das faixas nos desenhos, pois se houver inversão eles poderão queimar.
c) Para soldar C1, que é o capacitor eletrolítico, devemos também observar a sua polaridade, ou seja, a posição do sinal (+) ou (-) que vier marcado em seu invólucro.
d) Para soldar os resistores R1 e R2 é só preciso observar as cores das faixas que indicam seus valores. Para R3, que é de fio, não é preciso, pois a marcação é direta.
e) O leitor poderá agora fazer as ligações dos componentes externos, começando pelo potenciômetro que controla a corrente de eletrólise.
Este componente é ligado com três pedaços de fios, cujo comprimento deve ser verificado de acordo com a sua posição na caixa. Cuidado para não inverter a ordem de ligação destes fios.
f) O segundo componente externo que ligamos é o instrumento M, para o qual usamos dois pedaços de fio flexível. Este componente iá poderá estar fixado na caixa. A polaridade da ligação deve ser seguida. Se no instrumento que for usado não houver marcação de polaridade, inicialmente faça qualquer ligação, depois, no teste, se houver deflexão ao contrário, é só inverter os fios.
g) Na ligação do transformador devemos apenas tomar cuidado para não trocar os enrolamentos. O fio vermelho, marrom e preto corresponde ao primário que vai a S1 e ao cabo de alimentação. Se sua rede for de 110 V use os fios marrom e preto, e ser for de 220 V use os fios preto e vermelho. O secundário tem a tomada central de cor diferente dos extremos.
h) A ligação do cabo de alimentação e interruptor geral S1 é simples, não havendo nenhuma observação especial a ser feita. Apenas dê um nó no fio no ponto de entrada na caixa para evitar que um puxão mais forte cause seu rompimento.
i) Complete a montagem com a ligação dos bornes positivo e negativo de saída. Será conveniente usar um borne vermelho para o polo positivo e um preto para o negativo.
Se o potenciômetro atuar ao contrário, inverta seus fios extremos. Se o ponteiro atuar ao contrário, inverta os fios do medidor.
Se o transistor se aquecer em excesso, verifique novamente a sua montagem.
A ELETRÓLISE
Na figura 7 mostramos a maneira de se usar o aparelho numa eletrólise simples. Na introdução demos os elementos para que o leitor a realize.
Observamos que o hidrogênio produzido e um gás explosivo, Se, depois de recolher uma pequena quantidade deste no tubo de ensaio, o leitor aproximar um fósforo aceso vai ouvir um “pac" que representa uma pequena explosão.
Nesta explosão ocorre a combustão do hidrogênio que se combina com o oxigênio do ar formando novamente água.
Se o leitor aproximar um fósforo com a ponta em brasa do tudo de oxigênio, a chama se reativará, pois o oxigênio é comburente.
Experiências de galvanoplastia também poderão ser feitas com esta fonte.
Terminada a montagem, será fácil fazer um teste de funcionamento, mesmo sem material para a eletrólise.
TESTE
Ligue o cabo de alimentação à tomada, depois de conferir toda a montagem.
Acione S1 e observe se nenhum componente se aquece. Estando tudo em ordem, ligue nos bornes de saída (+) e (-) um resistor de 100 Ω x 5 W de fio, ou então uma lâmpada de 12 V x 500 mA ou menos corrente.
Girando o potenciômetro P1 no sentido de aumentar a corrente de saída, o ponteiro do instrumento deve registrar este fato, e se for usado resistor na saída, seu aquecimento será notado. No caso da lâmpada notaremos um aumento de sua luminosidade.
Q1 - transistor TlP31 ou equivalente, com dissipador de calor
D1, D2 -1N4002 ou BY127 - diodos de silício
Cl – 1 000 µF x 16 V ou mais - capacitor eletrolítico
P1 - 1k - potenciômetro simples
Ml - VU-meter de 200 µA
R1 - 330 Ω x ½ W - resistor (laranja, laranja, marrom)
R2 – 47 k x 1/8 W - resistor (amarelo, violeta, laranja)
R3 - 10 Ω x 10 W - resistor de fio
T1 - transformador com primário de acordo com a rede local e secundário de 12 + 12 V x 1 A.
S1 - interruptor simples
Diversos: ponte de terminais, base de montagem, caixa para montagem, bornes isolados, botão para o potenciômetro, fios, cabo de alimentação, solda, etc.
Artigo revisado em 2016